5. července zahájila společnost Novo Nordisk v Číně klinickou studii fáze III injekce CagriSema, jejímž účelem je porovnat bezpečnost a účinnost injekce CagriSema se semeglutidem u obézních pacientů a pacientů s nadváhou v Číně.
Injekce CagriSema je dlouhodobě působící kombinovaná terapie vyvíjená společností Novo Nordisk, hlavními složkami jsou agonista receptoru GLP-1 (glukagonu podobný peptid-1) smeglutid a dlouhodobě působící analog amylinu cagrilintid.Injekce CagriSema může být podávána subkutánně jednou týdně.
Primárním cílem bylo porovnat přípravek CagriSema (2,4 mg/2,4 mg) se semeglutidem nebo placebem jednou týdně subkutánně.Společnost Novo Nordisk oznámila výsledky studie přípravku CagriSema pro léčbu diabetu 2. stupně, která prokázala, že hypoglykemický účinek přípravku CagriSema je lepší než účinek semeglutidu a téměř 90 % subjektů dosáhlo cíle HbA1c.
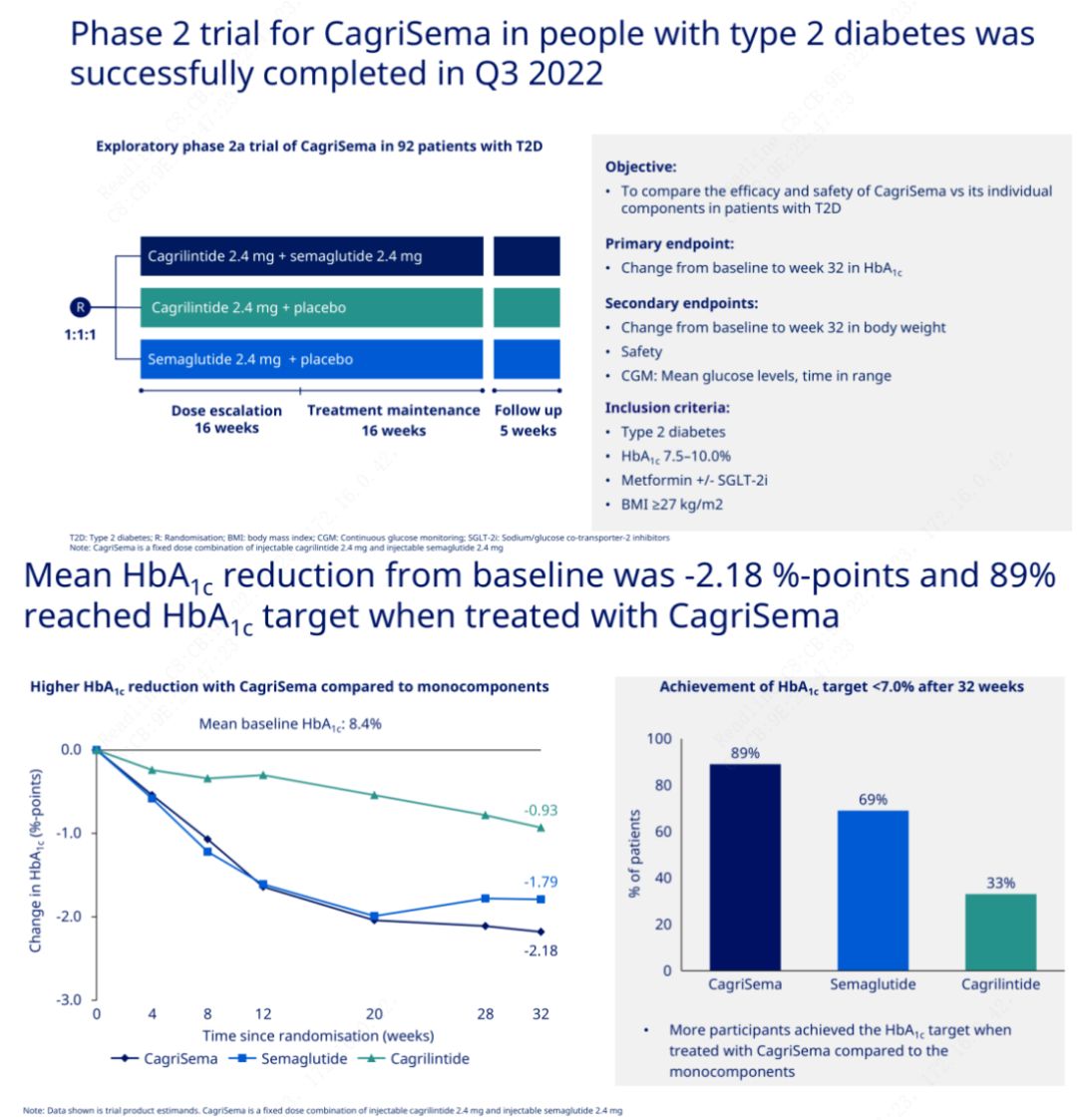
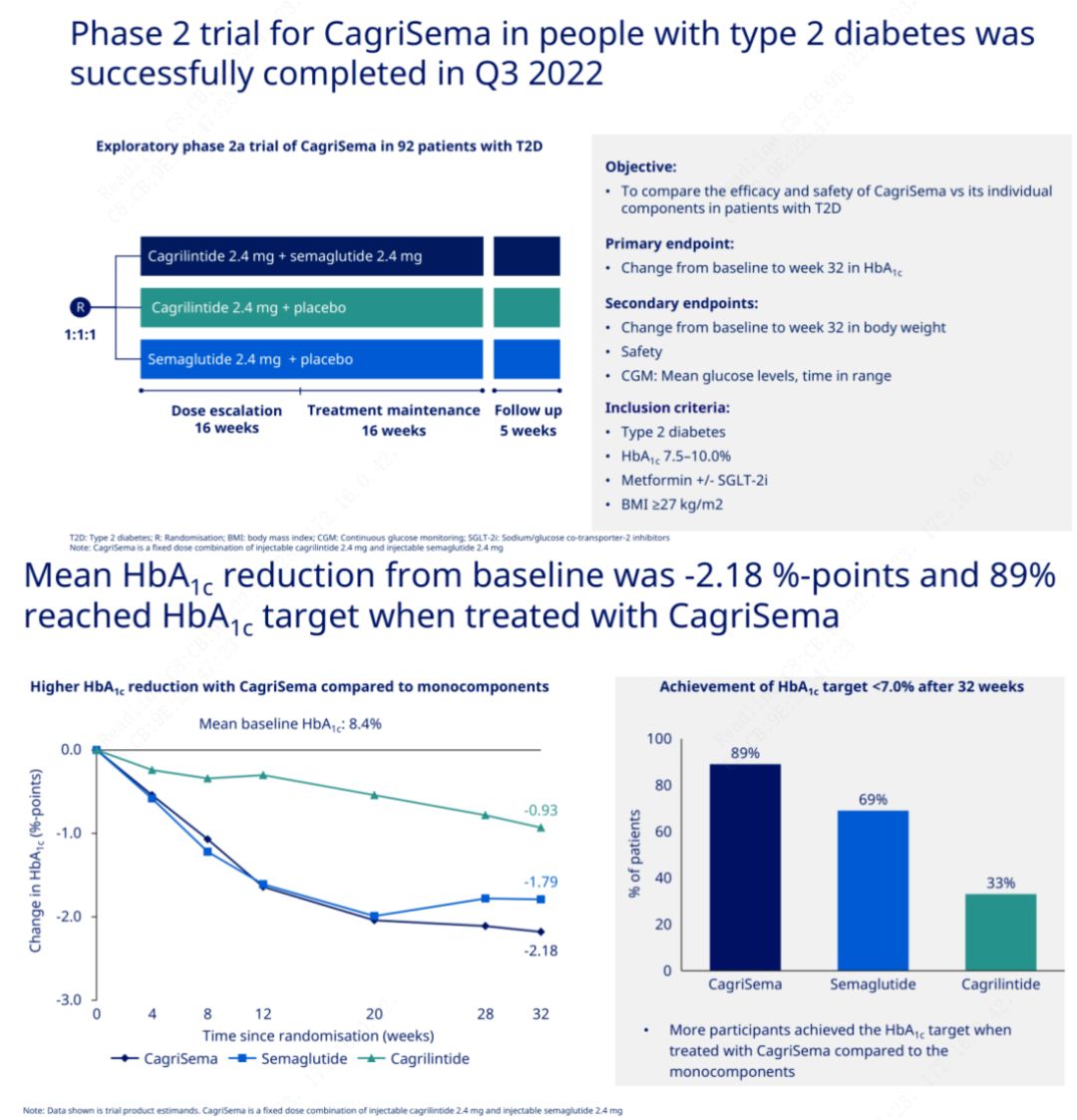
Data ukázala, že kromě významného hypoglykemického účinku, pokud jde o úbytek hmotnosti, injekce CagriSema výrazně překonala semeglutid (5,1 %) a cagrilintid (8,1 %) se ztrátou hmotnosti 15,6 %.
Inovativní lék Tirzepatid je celosvětově první schválený týdenní agonista GIP/GLP-1 receptoru.Kombinuje účinky dvou inkretinů do jediné molekuly, která se aplikuje jednou týdně, a je novou třídou léčby diabetu 2. typu.Tirzepatid byl schválen americkým Úřadem pro kontrolu potravin a léčiv (FDA) v květnu 2022 ke zlepšení kontroly glykémie (na dietním základě a cvičení) u dospělých s diabetem 2. typu a v současné době je schválen v Evropské unii, Japonsku a dalších zemích.
Dne 5. července společnost Eli Lilly oznámila studii SURPASS-CN-MONO fáze III o platformě pro registraci klinických studií a zveřejňování informací pro léčbu pacientů s diabetem 2. typu.SURPASS-CN-MONO je randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie fáze III navržená k vyhodnocení účinnosti a bezpečnosti monoterapie tirzepatidem ve srovnání s placebem u lidí s diabetem 2. typu.Studie plánovala zahrnout 200 pacientů s diabetem 2. typu, kteří neužívali žádná antidiabetika během 90 dnů před návštěvou 1 (s výjimkou určitých klinických situací, jako je akutní onemocnění, hospitalizace nebo plánovaný chirurgický zákrok, krátkodobý (≤14 dny) použití inzulínu).
Očekává se, že diabetes 2. typu bude schválen letos
Minulý měsíc byly výsledky studie SURPASS-AP-Combo zveřejněny 25. května v úspěšném časopise Nature Medicine.Výsledky ukázaly, že ve srovnání s inzulínem glargin vykazoval Tirzepatid lepší HbA1c a snížení hmotnosti v populaci pacientů s diabetem 2. typu v asijsko-pacifickém regionu (hlavně v Číně): snížení HbA1c až o 2,49 % a snížení hmotnosti až o 7,2 kg (9,4 %) po 40 týdnech léčby, významné zlepšení krevních lipidů a krevního tlaku a celková bezpečnost a snášenlivost byly dobré.
Fáze 3 klinické studie SURPASS-AP-Combo je první studií Tirzepatidu prováděnou převážně u čínských pacientů s diabetem 2. typu, kterou vedl profesor Ji Linong z Pekingské univerzitní lidové nemocnice.SURPASS-AP-Combo je v souladu s výsledky celosvětové série výzkumu SURPASS, která dále dokazuje, že patofyziologie diabetu u čínských pacientů je v souladu s patofyziologií diabetu u pacientů z celého světa, což je základem pro souběžný výzkum a vývoj nových léků v Číně a ve světě a také poskytuje solidní důkazní podporu pro to, aby čínským pacientům poskytla příležitost používat nejnovější léky na léčbu cukrovky a jejich klinické použití v Číně co nejdříve.
Čas odeslání: 18. září 2023

